Bài học liên quan
Phần 1
(27 câu)Phản ứng thuận nghịch là phản ứng theo …(1)… trái ngược nhau trong …(2)… điều kiện. Nội dung phù hợp với ô trống (1) và (2) là
Xét phản ứng: C(s)+CO2(g)⇌2CO(g). Biểu thức hằng số cân bằng của phản ứng trên là
Dung dịch nào sau đây có pH nhỏ nhất? (Giả sử các dung dịch này có cùng số mol chất tan và cùng thể tích)
Theo thuyết Brønsted – Lowry, chất nào sau đây là thuộc loại chất lưỡng tính?
Có thể sử dụng quỳ tím để nhận biết ba dung dịch nào sau đây?
Trong tự nhiên, nitrogen tồn tại ở hai dạng đồng vị là
Chất nào sau đây vừa có tính oxi hóa, vừa có tính khử?
Đạm ammonium sulfate có thành phần chính là
Hòa tan hoàn toàn 16,8 gam một kim loại X (hóa trị II) vào dung dịch HNO3 đặc, nóng. Sau khi kết thúc phản ứng, chỉ thu được 34,7 L (đkc) khí màu nâu đỏ. Kim loại X là
Khi đeo bạc lâu ngày, bạc thường bị xỉn màu là do
Để pha loãng dung dịch sulfuric acid, ta cần
Trong quá trình sản xuất sulfuric acid bằng phương pháp tiếp xúc, phản ứng nào cần thực hiện ở áp suất cao để tăng hiệu suất phản ứng?
Hợp chất nào sau đây thuộc loại dẫn xuất halogen?
Glutamic acid là thành phần quan trọng trong quá trình tổng hợp protein, đồng thời đóng vai trò chính trong việc kích hoạt thần kinh. Công thức cấu tạo dạng mạch khung của glutamic acid như hình dưới đây:
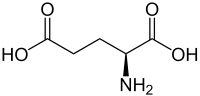
Công thức phân tử của glutamic acid là
Công thức nào sau đây không phải là đồng phân ứng với C5H12?
Có thể sử dụng phương pháp chiết để tách hỗn hợp nào sau đây?
Dùng thông tin sau để trả lời các Câu 1 và Câu 2: Tiến hành thí nghiệm sau trong một ống xi-lanh:
2NO2(g) | ⇌ | N2O4(g) |
màu nâu đỏ |
| không màu |
Biểu thức hằng số cân bằng của hệ phản ứng là
Khi đẩy pít-tông xuống để làm giảm thể tích, màu sắc của hỗn hợp trong xi-lanh sẽ thay đổi như thế nào?
Tiến hành thử tính dẫn điện của ba dung dịch A, B, C và thu được kết quả như sau:
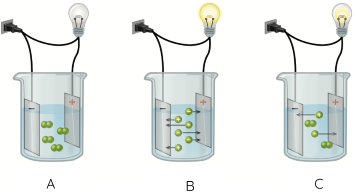
| a) Dung dịch C có khả năng dẫn điện tốt hơn dung dịch A. |
|
| b) Dung dịch A có chứa chất điện li yếu. |
|
| c) Dung dịch C có khả năng phân li hoàn toàn ra ion. |
|
| d) Dung dịch B có thể có chứa muối của sodium. |
|
Ammonia được sản xuất từ quá Haber - Bosch theo hệ phản ứng sau:
N2(g)+3H2(g)⇌to,xt,p2NH3(g)
với ΔrH298o=−91,8 kJ
(Nhấp vào ô màu vàng để chọn đúng / sai)| a) Phản ứng tổng hợp ammonia là phản ứng thuận nghịch. |
|
| b) Tại thời điểm cân bằng, thu được hỗn hợp gồm ba khí là nitrogen, hydrogen và ammonia. |
|
| c) Nếu tăng áp suất, cân bằng sẽ chuyển dịch theo chiều nghịch. |
|
| d) Năng lượng liên kết trong phân tử N2 là 934,2 kJ/mol (Biết năng lượng liên kết H-H và N-H lần lượt là 436,0 kJ/mol và 389,0 kJ/mol). |
|
Tiến hành đo phổ hồng ngoại của hợp chất hữu cơ X thu được kết quả như sau:
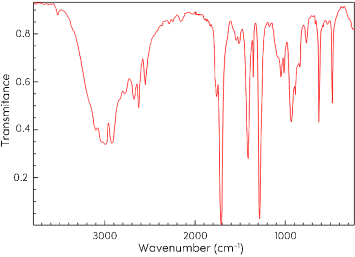
| a) Trong X có chứa liên kết O-H. |
|
| b) Tín hiệu phổ ở khoảng 1760 – 1690 cm-1 là của liên kết C=O. |
|
| c) X thuộc loại dẫn xuất hydrocarbon. |
|
| d) X là đồng đẳng của CH3CH2OH. |
|
Tiến hành điều chế ethyl acetate theo sơ đồ thí nghiệm sau:
C2H5OH+CH3COOH⇌H+,toCH3COOC2H5+H2O
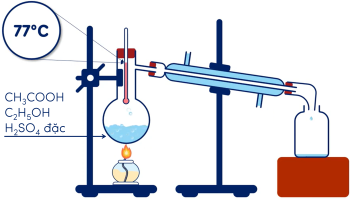
| a) Phản ứng điều chế ethyl acetate là phản ứng thuận nghịch. |
|
| b) Nếu tăng áp suất của phản ứng thì cân bằng chuyển dịch theo chiều thuận. |
|
| c) Quá trình điều chế ethyl acetate dựa trên phương pháp chưng cất thường. |
|
| d) Hỗn hợp thu được sau phản ứng chứa acetic acid và nước. |
|
Cho các phản ứng thuận nghịch sau:
(1)Fe2O3(s)+3CO(g)⇌2Fe(s)+3CO2(g)
(2)2NO2(g)⇌N2O4(g)
(3)2C(s)+O2(g)⇌2CO(g)
(4)HCOOH(l)+CH3OH(l)⇌H+,toHCOOCH3(l)+H2O(aq)
Nếu tăng áp suất của hệ thì phản ứng nào có cân bằng chuyển dịch theo chiều thuận?
Trả lời: .
Tiến hành thí nghiệm sau: Lấy 10 mL dung dịch HCl 1 M cho tác dụng với 10 mL dung dịch NH3 0,5 M. Để chuẩn độ lượng HCl dư sau phản ứng cần phải dùng a mL dung dịch NaOH 1 M. Tìm giá trị của a.
Trả lời: .
Caffeine là chất kích thích tự nhiên được tìm thấy trong cây trà, cà phê, ca cao. Khi dung nạp vào cơ thể, caffeine sẽ kích thích não và hệ thần kinh trung ương, giúp con người tỉnh táo và ngăn ngừa mệt mỏi. Tiến hành đo phổ MS của caffeine thu được kết quả như hình dưới đây:
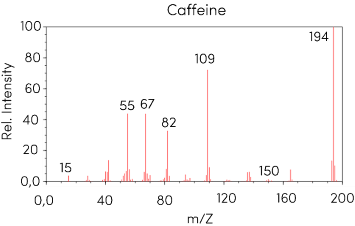
Khối lượng phân tử của caffeine là bao nhiêu g/mol?
Trả lời: .
Cho dãy các chất: CO2, NH3, CH4, C2H2, C6H5, CaCO3, CCl4, CS2. Có bao nhiêu hợp chất hữu cơ trong dãy trên?
Trả lời: .
Hình ảnh dưới đây mô tả các bước tiến hành khi kết tinh chất rắn (không được đánh số theo thứ tự thực hiện):
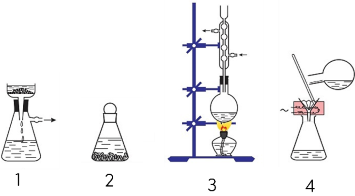
Xác định thứ tự các bước thực hiện đúng (viết liền không dấu).
Trả lời: .
Có bao nhiêu đồng phân cấu tạo ứng với công thức C4H10?
Trả lời: .