Bài học liên quan
Phần 1
(40 câu)Phản ứng nào dưới đây là phản ứng thuận nghịch?
Quan sát hình sau và chọn phát biểu đúng.
.png)
Cho các phản ứng sau:
| (1) N2O4 (g) ⇌ 2NO2 (g) | KC = 0,2 |
| (2) H2 (g) + I2 (g) ⇌ 2HI (g) | KC = 50 |
| (3) CO2 (g) + H2 (g) ⇌ CO (g) + H2O (g) | KC = 0,659 |
| (4) PCl3 (g) + Cl2 (g) ⇌ PCl5 (g) | KC = 34 |
Dựa vào giá trị hằng số cân bằng, phản ứng nào có hiệu suất cao nhất?
Cho vào bình kín (dung tích 1L) 1 mol H2 và 1 mol I2. Thực hiện phản ứng ở 350 - 500oC theo phương trình hóa học:
H2 (g) + I2 (g) ⇌ 2HI (g)
Ở trạng thái cân bằng thấy có sự tạo thành 1,56 mol HI. Tính hằng số cân bằng của phản ứng trên.
Trong dung dịch muối Fe3+ tồn tại cân bằng sau: Fe3+ + 3H2O ⇌ Fe(OH)3↓ + 3H+. Để bảo quản dung dịch Fe3+, người ta sẽ thêm vào bình đựng vài giọt dung dịch chứa ion nào dưới đây?
Trong dung dịch muối CoCl2 (màu hồng) tồn tại cân bằng hóa học sau:
|
[Co(H2O)6]2+ + 4Cl- ⇌ [CoCl4]2- + 6H2O |
ΔrHo298 > 0 |
| màu hồng màu xanh |
Màu sắc của ống nghiệm đựng dung dịch CoCl2 sẽ thay đổi như thế nào nếu thêm từ từ dung dịch HCl đặc vào ống nghiệm?
Cho các chất: NaOH, HCl, HNO3, NaNO3, saccharose (C12H22O11), ethanol (C2H5OH), glycerol (C3H5(OH)3), KAl(SO4)2.12H2O. Trong các chất trên, có bao nhiêu chất tạo được dung dịch dẫn điện?
Chất/ion nào trong các chất/ion dưới đây là base theo thuyết acid - base của Bronsted - Lowry?
Trộn 40 ml dung dịch H2SO4 0,25 M với 60 ml dung dịch NaOH 0,5 M. pH của dung dịch thu được là
Thêm nước vào 10 mL dung dịch HCl 0,1 M để thu được 1000 mL dung dịch A. Dung dịch mới thu được có pH thay đổi như thế nào so với dung dịch ban đầu?
Trong các oxide của nitrogen, oxide nào thu được thông qua phản ứng giữa nitrogen và oxygen?
Công thức cấu tạo của phân tử nitrogen là
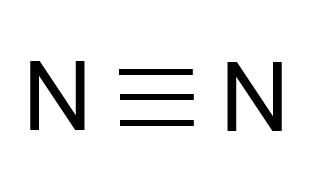
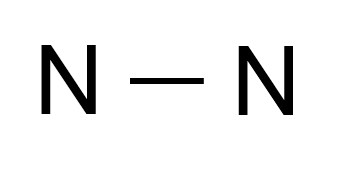
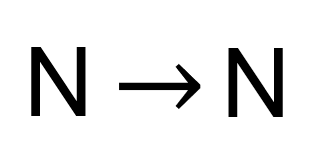
Để phân biệt các dung dịch NH4Cl, (NH4)2SO4, NaCl, Na2SO4, chỉ cần sử dụng một thuốc thử duy nhất là
Trong phân tử NH4NO3, số oxi hóa của nguyên tử nitrogen là
Mưa acid là hiện tượng nước mưa có pH thấp hơn 5,6 (giá trị pH của khí carbon dioxide bão hòa trong nước). Hai tác nhân chính gây mưa acid là
Ammonium nitrate là một loại phân bón giàu dinh dưỡng, được sản xuất theo phản ứng hóa học sau:
NH3 + HNO3 → NH4NO3
Trong phản ứng này, nitric acid đóng vai trò là
Trong công nghiệp, người ta sản xuất nitric acid theo sơ đồ sau: NH3 → NO → NO2 → HNO3
Hiệu suất của quá trình trên là 96,2%. Để điều chế 200 000 tấn nitric acid nồng độ 60% cần dùng bao nhiêu tấn NH3?
Tính chất nào sau đây không phải tính chất vật lí của sulfur?
Sulfur đóng vai trò là chất khử khi phản ứng với chất nào dưới đây?
Giai đoạn thứ hai của quá trình sản xuất sulfuric acid là giai đoạn chuyển hóa từ SO2 thành SO3 theo phản ứng: 2SO2 (g) + O2 (g) ⇌ 2SO3 (g) ΔrHo298 = -197,6 kJ với xúc tác vanadium (V) oxide. Để tăng hiệu suất tạo thành SO3, cần
Dung dịch nào sau đây có thể gây bỏng khi rơi vào da?
Kết quả phân tích thành phần của một muối sulfate có thấy nguyên tố kim loại M chiếm 28% về khối lượng, còn lại là oxygen và lưu huỳnh. Kim loại M là
Tính chất nào sau đây không phải tính chất hóa học của sulfuric acid?
Sử dụng phương pháp chưng cất để tách hỗn hợp các alkane: pentane (ts = 36,1oC), heptane (ts = 98,4oC), octane (ts = 125,7oC) và nonane (ts = 150,8oC). Alkane được tách ra đầu tiên là
Tách hai chất lỏng tan vào nhau bằng phương pháp chưng cất dựa trên sự khác nhau của hai chất về
Để tách riêng từng chất ra khỏi hỗn hợp benzene và aniline, người ta sử dụng phương pháp nào? Biết nhiệt độ sôi của benzene và aniline lần lượt là 80,1oC và 184,1oC.
Hai hợp chất A và B có cùng công thức thực nghiệm là CH2O. Phổ MS cho thấy A và B có các tín hiệu sau.
|
Chất A
|
Chất B
|
Biết mảnh [M+] có m/z lớn nhất.
Công thức phân tử của chất A và chất B lần lượt là
Khi biết công thức thực nghiệm, có thể xác định công thức phân tử của hợp chất hữu cơ dựa vào đặc điểm nào dưới đây?
Nhận xét nào dưới đây về hai công thức cấu tạo bên là đúng?
.png)
Quang hợp là quá trình cây sử dụng nước và khí carbon dioxide lấy từ môi trường, nhờ năng lượng ánh sáng được diệp lục hấp thụ, tổng hợp glucose và giải phóng khí oxygen. Glucose có cấu tạo ở hình dưới.
Có bao nhiêu loại nhóm chức trong phân tử glucose?
Hợp chất A có công thức phân tử C3H6O. Khi đo phổ hồng ngoại cho kết quả như hình bên.
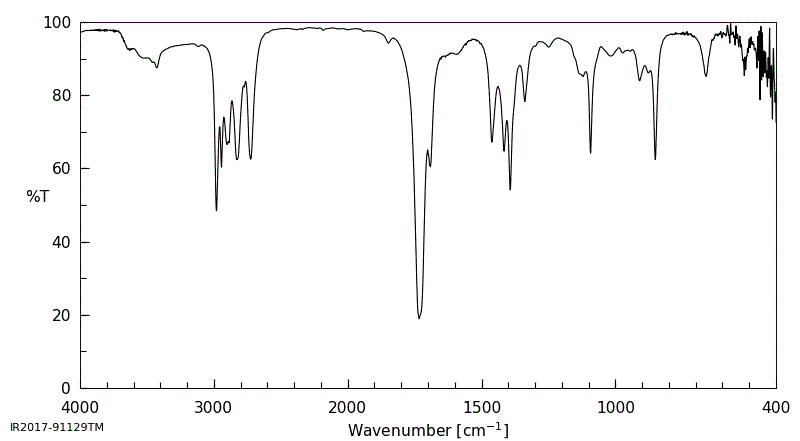
Công thức cấu tạo của A là
Để có được một số hoạt chất trong thảo dược để bồi bổ cơ thể hoặc trị bệnh, người ta có thể lấy thảo dược đi "sắc thuốc" hoặc "ngâm rượu thuốc". Phương pháp tách nào đã được sử dụng trong việc làm này?
Độ tan trong nước của monosodium glutamate (mì chính hay bột ngọt) ở 60oC là 112 g/100 g nước; ở 25oC là 74 g/100 g nước. Khi làm nguội 212 gam dung dịch monosodium glutamate bão hòa ở 60oC xuống 25oC thì khối lượng monosodium glutamate kết tinh thu được là
Saccharose (hay sucrose) là loại đường được tách ra từ cây mía hoặc củ cải đường, được sử dụng rất phổ biến trong công nghiệp thực phẩm. Phân tích nguyên tố sucrose, thu được kết quả như sau: 42,11% C; 6,43% H và 51,46% O. Phổ MS của sucrose cho thấy peak ion phân tử có m/z bằng 342. Công thức phân tử của sucrose là
Số đồng phân mạch hở ứng với công thức phân tử C3H6Br2 là
Có bao nhiêu đồng phân mạch hở có công thức phân tử C3H8O?
Phát biểu nào dưới đây đúng khi nói về thuyết cấu tạo hóa học?
Cho các phản ứng sau:
(1) H2 + O2 → H2O
(2) 2KMnO4 → K2MnO4 + MnO2 + O2
(3) 3H2 + N2 ⇌ 2NH3
(4) NaOH + HCl → NaCl + H2O
(5) CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O
(6) C + CO2 ⇌ CO
Số phản ứng thuận nghịch là
Hoàn thành phát biểu sau về nguyên lí chuyển dịch cân bằng Le Chatelier bằng cách lựa chọn từ thích hợp điền vào chỗ trống.
"Một phản ứng ...(1)... đang ở trạng thái cân bằng khi chịu một tác động từ bên ngoài như biến đổi nồng độ, áp suất, nhiệt độ, thì cân bằng sẽ chuyển dịch theo chiều làm ...(2)... tác động bên ngoài đó."
Vàng tan trong hỗn hợp dung dịch nitric acid đặc và dung dịch hydrochloric acid đặc (tỉ lệ 1 : 3) về thể tích tạo ra hợp chất tan của của Au theo phản ứng sau:
Au + HNO3 + HCl → HAuCl4 + NO + H2O.
Tổng hệ số các chất trong phản ứng là
