Bài học liên quan
Phần 1
(27 câu)Nguyên tử sodium có 11 proton trong hạt nhân. Số đơn vị điện tích hạt nhân của nguyên tử này là bao nhiêu?
Liên kết pi (π) được tạo thành từ sự xen phủ
Cho phổ MS của iron (sắt) như sau:
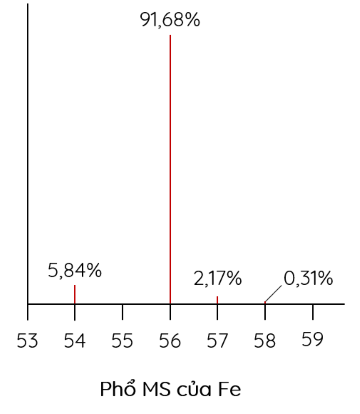
Trong tự nhiên, iron có bao nhiêu đồng vị bền?
“Năng lượng liên kết là năng lượng cần thiết để ...(1)... một liên kết hóa học trong phân tử ở thể ...(2)... thành nguyên tử ở thể khí.” Từ/cụm từ thích hợp để điền vào (1) và (2) lần lượt là
Trong bảng tuần hoàn các nguyên tố hóa học, nhóm bao gồm các nguyên tố mà trong nguyên tử có cùng số
Liên kết hóa học là sự kết hợp giữa
Khi tham gia liên kết hóa học, nguyên tử Mg có xu hướng nhường 2 electron để hình thành ion
Từ vị trí của nguyên tố trong bảng tuần hoàn, không thể xác định/dự đoán được
Chất nào dưới đây tạo được liên kết hydrogen với nước?
Độ âm điện là đại lượng đặc trưng cho khả năng nào của nguyên tử?
Nối dung dịch sodium chloride với nguồn điện và một bóng đèn nhỏ. Quan sát thấy bóng đèn
Sử dụng thông tin sau cho Câu 1 và Câu 2: Cho các nguyên tố hóa học sau: O (Z = 8), Na (Z = 11), Al (Z = 13), S (Z = 16), Cl (Z = 17), Ca (Z = 20).
Dãy nào dưới đây gồm các nguyên tử có xu hướng tham gia liên kết hóa học để đạt được cấu hình electron bền của khí hiếm argon (Z = 18)?
Chất nào dưới đây là hợp chất cộng hóa trị?
Nguyên tố X nằm ở nhóm A trong bảng tuần hoàn. Hợp chất của X có nhiều ứng dụng trong đời sống như làm thuốc đánh răng, chế tạo dụng cụ nhà bếp, sử dụng trong quá trình sản xuất nhôm,... Hợp chất khí của X với hydrogen có công thức hóa học là HX. X nằm ở nhóm mấy trong bảng tuần hoàn?
Nguyên tố A được sử dụng trong nhiều ngành công nghiệp: gốm, men sứ, thủy tinh, luyện thép, vật liệu bán dẫn,... Trong nguyên tử nguyên tố A có 44 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện 12 hạt. Phát biểu nào dưới đây không đúng khi nói về nguyên tố A?
Dãy nào dưới đây bao gồm các chất được sắp xếp theo chiều tăng dần nhiệt độ sôi?
Sulfur (S) là nguyên tố phổ biến thứ 17 trên vỏ Trái Đất, chiếm khoảng 0,03 – 0,1% khối lượng. Trong cơ thể người, sulfur chiếm khoảng 0,2% khối lượng, có trong thành phần nhiều protein và enzyme. Trong bảng tuần hoàn các nguyên tố hóa học, sulfur nằm ở ô số 16. Phát biểu nào dưới đây đúng?
Carbon dioxide (CO2) là hợp chất khí ở điều kiện thường, là nguyên liệu của quá trình quang hợp ở thực vật để tổng hợp chất hữu cơ. Khí này có mặt trong khí quyển Trái Đất với nồng độ thấp và tác động như một khí gây hiệu ứng nhà kính và là thành phần chính trong chu trình carbon. Cho phổ MS của carbon và oxygen như sau:

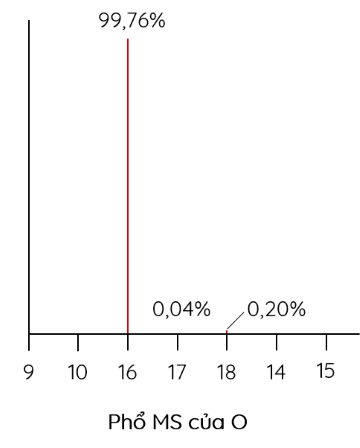
| a) Trong tự nhiên, oxygen có ba đồng vị bền là 16O, 17O, và 18O. |
|
| b) Có ba loại carbon dioxide được tạo nên các đồng vị của carbon và oxygen. |
|
| c) Khối lượng phân tử của carbon dioxide là 44,00 amu. |
|
| d) Trong carbon dioxdie, 16O chiếm 72,53% về khối lượng. |
|
Nguyên tố phosphorus (P, Z = 15) và chlorine (Cl, Z = 17) đều thuộc chu kì 3 trong bảng tuần hoàn các nguyên tố hóa học.
(Nhấp vào ô màu vàng để chọn đúng / sai)| a) Nguyên tử phosphorus và chlorine đều có 2 lớp electron. |
|
| b) Phosphin là hợp chất khí với hydrogen của phosphorus, có công thức là PH3. |
|
| c) Trong oxide ứng với hóa trị cao nhất của chlorine, oxygen chiếm 11,41% về khối lượng. |
|
| d) HClO4 có tính acid mạnh hơn H3PO4. |
|
Formic acid là carboxylic acid đơn giản nhất, có công thức phân tử là CH2O2. Trong tự nhiên, formic acid có trong các vòi đốt và nọc độc của nhiều loại côn trùng như ong, kiến,... Công thức cấu tạo của formic acid như sau:
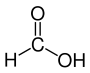
| a) Các liên kết trong formic acid đều là liên kết cộng hóa trị không phân cực. |
|
| b) Liên kết đôi giữa carbon và oxygen trong formic acid được hình thành do sự xen phủ bên p – p. |
|
| c) Trong phân tử formic acid có 2 liên kết sigma (σ) hình thành do sự xen phủ trục p – p. |
|
| d) Formic acid là chất cộng hóa trị nên ít tan trong nước. |
|
Cho các nguyên tố sau: fluorine (F, Z = 9), chlorine (Cl, Z = 17), bromine (Br, Z = 35) và iodine (I, Z = 53). Các nguyên tố này thuộc nhóm halogen, là nhóm phi kim điển hình. Các nguyên tố halogen thường được kí hiệu là X.
(Nhấp vào ô màu vàng để chọn đúng / sai)| a) Nhóm halogen là nhóm VIA trong trong bảng tuần hoàn các nguyên tố hóa học. |
|
| b) Các nguyên tử halogen đều có xu hướng nhận thêm hoặc góp chung 1 electron khi tham gia liên kết hóa học. |
|
| c) Oxide ứng với hóa trị cao nhất của halogen là X2O7, hợp chất khí với hydrogen là HX. |
|
| d) Trong dãy hydrogen halide HX, hydrogen iodide có nhiệt độ nóng chảy và nhiệt độ sôi cao nhất do tương tác van der Waals mạnh nhất. |
|
Cho các nguyên tố hóa học có số hiệu nguyên tử là 5, 8, 9, 17. Trong các nguyên tố này, nguyên tố có độ âm điện lớn nhất có số hiệu nguyên tử là bao nhiêu?
Trả lời: .
Nitrogen là nguyên tố hóa học có mặt trong tất cả các cơ thể sống, chủ yếu ở dạng các amino acid (hoặc protein), có trong các nucleic acid (DNA và RNA). Trong hạt nhân nguyên tử nitrogen có 7 proton. Cho các phát biểu sau về nitrogen:
(1) Nitrogen là nguyên tố kim loại.
(2) Nitrogen có 3 electron độc thân.
(3) Nguyên tử nitrogen có 2 lớp electron.
(4) Nitrogen nằm ở chu kì 3, nhóm VA trong bảng tuần hoàn.
(5) Phân lớp ngoài cùng của nitrogen là 2p.
Liệt kê các phát biểu đúng theo thứ tự từ lớn đến bé (ví dụ: 542, 4321,...)
Trả lời: .
Nguyên tố kim loại M là nguyên tố kim loại phổ biến nhất trong vỏ Trái Đất. Trong bảng tuần hoàn các nguyên tố hóa học, M nằm ở chu kì 3, nhóm IIIA. Trong tự nhiên, M chỉ có một đồng vị ổn định, đồng vị này có 14 neutron trong hạt nhân. Số khối của đồng vị này là bao nhiêu?
Trả lời: .
Cho các chất sau: NaCl, MgO, CO2, HCl, H2SO4, CaCO3, Li3N, KNO3. Có bao nhiêu chất trong phân tử chỉ chứa liên kết ion?
Trả lời: .
Trong tự nhiên, magnesium có 3 đồng vị bền là 24Mg, 25Mg và 26Mg. Trong đó, đồng vị 24Mg có phần trăm số nguyên tử lớn nhất là 78,99%. Nguyên tử khối trung bình của magnesium là 24,305. Phần trăm số nguyên tử của đồng vị 25Mg là bao nhiêu?
(Làm tròn kết quả đến hàng phần mười.)
Trả lời: .
Trong phân tử sulfuric acid (H2SO4), nguyên tử S liên kết với 4 nguyên tử O, trong đó có 2 nguyên tử O liên kết với 2 nguyên tử H. Hóa trị của nguyên tố S trong H2SO4 là n, bằng tổng số liên kết σ và liên kết π mà S tạo được với các nguyên tử xung quanh. Biết số hiệu nguyên tử của H, O và S lần lượt là 1, 8 và 16. Giá trị của n là bao nhiêu?
Trả lời: .